Propiedades físicas de los ácidos carboxílicos.
Los ácidos carboxílicos hierven a temperaturas muy superiores que los alcoholes, cetonas o aldehídos de pesos moleculares semejantes. Los puntos de ebullición de los ácidos carboxílicos son el resultado de la formación de un dímero estable con puentes de hidrógeno.
- Puntos de ebullición.
Los ácidos carboxílicos que contienen más de ocho átomos de carbono, por lo general son sólidos, a menos que contengan dobles enlaces. La presencia de dobles enlaces (especialmente dobles enlaces cis) en una cadena larga impide la formación de una red cristalina estable, lo que ocasiona un punto de fusión más bajo.
Los puntos de fusión de los ácidos dicarboxílicos son muy altos. Teniendo dos carboxilos por molécula, las fuerzas de los puentes de hidrógeno son especialmente fuertes en estos diácidos: se necesita una alta temperatura para romper la red de puentes de hidrógeno en el cristal y fundir el diácido.
- Puntos de fusión.
Los ácidos carboxílicos forman puentes de hidrógeno con el agua, y los de peso molecular más pequeño (de hasta cuatro átomos de carbono) son miscibles en agua. A medida que aumenta la longitud de la cadena de carbono disminuye la solubilidad en agua; los ácidos con más de diez átomos de carbono son esencialmente insolubles.
3. Solubilidad.
Los ácidos carboxílicos son muy solubles en los alcoholes, porque forman enlaces de hidrógeno con ellos. Además, los alcoholes no son tan polares como el agua, de modo que los ácidos de cadena larga son más solubles en ellos que en agua. La mayor parte de los ácidos carboxílicos son bastante solubles en solventes no polares como el cloroformo porque el ácido continua existiendo en forma dimérica en el solvente no polar. Así, los puentes de hidrógeno de dímero cíclico no se rompen cuando se disuelve el ácido en un solvente polar.
Los puntos de ebullición y fusión de los ácidos carboxílicos son en general mucho más altos de lo que les correspondería para un peso molecular dado. Esto se explica porque forman dímeros, en el que un grupo CO2H se une muy fuertemente a otro mediante dos enlaces de hidrógeno. De esta forma, la molécula tiene un peso aparente doble y su punto de fusión y ebullición aumentan acordes a este fenómeno.
Grupos Funcionales. Ácidos Carboxílicos.
Atomos involucrados |  |
Suffijo | Acido -oico |
Prefijo | carboxi |
Posición en la cadena | Solo al final de la cadena |
Fórmula General | CnH2nO2 |
Nombre de la familia | Acidos carboxílicos |
Notes:
- Se nombran cambiando la terminación o de los alcanos por la terminacion oico
- En este caso el nombre de la IUPAC para este tipo de compuestos contiene dos palabras el prefijo ácido y el sufijo -oico.
- El grupo carbonilo siempre se va a encontrar al final de la cadena por lo que el número localizados no es necesario..
El comportamiento químico de los ácidos carboxílicos esta determinado por el grupo carboxilo -COOH. Esta función consta de un grupo carbonilo (C=O) y de un hidroxilo (-OH). Donde el -OH es el que sufre casi todas las reacciones: pérdida de protón (H+) o reemplazo del grupo –OH por otro grupo. | ||||||||||||||||||||||||
| ||||||||||||||||||||||||
Constantes de acidez de algunos ácidos carboxílicos
Síntesis de los ácidos carboxílicos | ||||||||||||||||||||||||
Los ácidos carboxílicos pueden obtenerse a partir de reacciones químicas como la oxidación de alcoholes primarios, de los compuestos alquil-bencénicos y por la hidrólisis de nitrilos entre otras. | ||||||||||||||||||||||||
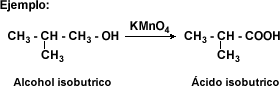
Oxidación de alcoholes primarios: para obtener ácidos carboxílicos mediante esta reacción, el alcohol primario se trata con un agente oxidante fuerte donde el alcohol actúa como un agente reductor oxidándose hasta ácido carboxílico.
| ||||||||||||||||||||||||
Oxidación de los compuestos alquil-bencénicos: la oxidación de los derivados alquil-bencénicos con mezclas oxidantes fuertes llevan a la formación de ácidos carboxílicos.
| ||||||||||||||||||||||||
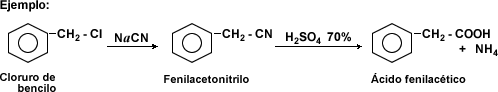
Hidrólisis de Nitrilos: los nitrilos se hidrolizan al ser sometidos a ebullición con ácidos minerales o álcalis en solución acuosa, generando ácidos carboxílicos mediante sustitución nucleofílica.
| ||||||||||||||||||||||||
| Derivados de los Ácidos Carboxílicos: Los derivados carboxílicos son compuestos que presentan el grupo acilo o el grupo aroilo en los ácidos alifáticos o aromáticos. | |||||||||||||||||||||||
Entre los derivados de los ácidos carboxílicos se encuentran: las sales de ácido, los ésteres, los haluros de ácidos, anhídridos de ácidos, amidas e imidas. | ||||||||||||||||||||||||
Propiedades físicas de los derivados de ácidos carboxílicos: | ||||||||||||||||||||||||
Los ésteres no presentan puentes de hidrógeno intermolecular por lo que sus puntos de ebullición son similares a los de los alcanos de pero molecular similar. A partir de los tres átomos de carbono, su solubilidad en agua disminuye. Se disuelven bien en solventes orgánicos. Los más volátiles tienen olores agradables. Se usan en perfumería y para preparar condimientos artificiales. |
| |||||||||||||||||||||||
| Haluros de ácido: La mayor importancia la tienen los cloruros de ácido. El primer miembro de la serie alifática es el cloruro de metanoilo o cloruro de formilo, el cual es un compuesto inestable. | |||||||||||||||||||||||
La mayoría son líquidos de bajo punto de fusión y olores irritantes. No presentan puente de hidrógeno intermolecular, por lo que sus puntos de ebullición son más bajos que los de los ácidos de los que se derivan. | ||||||||||||||||||||||||
Anhídridos de ácido: En este grupo sólo tiene importancia el anhídrido etanóico, que es un compuesto polar, no presenta puente de hidrógeno intermolecular por ser el producto de la deshidratación de dos moles de ácido carboxílico. Sus puntos de ebullición son similares a los de los aldehídos y cetonas de peso molecular semejante. |
| |||||||||||||||||||||||
| El primer miembro de la serie alifática es la metanamida o formamida que es diluida a temperatura ambiente, el resto de las amidas son sólidas. Presentan un puente de hidrógeno intermolecular por lo que sus puntos de ebullición son altos. | |||||||||||||||||||||||
| Son compuestos polares, lo cual junto con la formación de puente de hidrógeno con el agua las hace solubles en esta. La solubilidad disminuye a partir de los cinco carbonos, debido a que la relación carbono – amino es mayor que 3:1. La etanamida y sus homólogos son excelentes solventes orgánicos. | ||||||||||||||||||||||||
ACIDEZ.
La propiedad más característica de los ácidos carboxílicos es la acidez del hidrógeno situado sobre el grupo hidroxilo. El pKa de este hidrógeno oscila entre 4 y 5 dependiendo de la longitud de la cadena carbonada
El ácido metanoico, también llamado ácido fórmico, es un ácido orgánico de un solo átomo de carbono, y por lo tanto el más simple de los ácidos orgánicos. Su fórmula es H-COOH (CH2O2), el grupo carboxilo es el que le confiere las propiedades ácidas a la molécula. Su base conjugada se ve estabilizada por dos estructuras de resonancia, favoreciendo su acidez.
El pKa del ácido fórmico es de 3,75. Teniendo en cuenta que el pH varía generalmente entre 0 y 14 (siendo 7 el pH neutro) podríamos decir que el fórmico, pese a ser un ácido de origen natural es relativamente fuerte.
Entre otras propiedades el ácido metanoico es un ácido líquido, incoloro, de olor irritante, con punto de ebullición de 100,7 °C y de congelación de 8,4 °C y es completamente soluble en agua pues su cadena carbonada es muy corta y fácilmente ionizable.
En el agua el ácido metanoico se disocia, reaccionando de la siguiente manera:
Cuando se manipule ácido formico hay que hacerlo con guantes, ya que este en contacto con la piel produce rápidamente ampollas dolorosas que se revientan y sangran.
Este ácido es el que inyectan las hormigas al morder. De ahí el nombre de fórmico (del latín formica, hormiga).
acido acetico.
ácido acético también es mejor conocido como ácido metilencarboxílico, se puede encontrar en forma de ion acetato. Éste es un ácido que se encuentra en el vinagre, siendo el principal responsable de su sabor y olor agrios. Su fórmula es CH3-COOH (C2H4O2). De acuerdo con la IUPAC se denomina sistemáticamente ácido etanoico.
acido benzoico.
ACIDO BENZOICO
El ácido benzoico es un ácido carboxílico aromático que tiene un grupo carboxilo unido a un anillo fenílico.En condiciones normales se trata de un sólido incoloro con un ligero olor característico. Es poco soluble en agua fría pero tiene buena solubilidad en agua caliente o disolventes orgánicos.
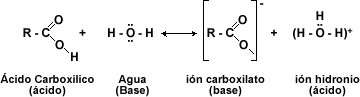
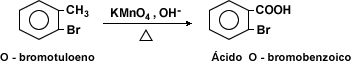
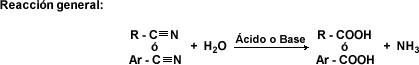
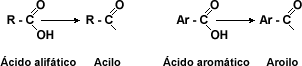

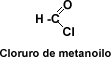
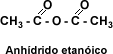





No hay comentarios:
Publicar un comentario